2024年12月30日,我校动科学院刘玉兰教授团队在Journal of Advanced Research(中科院1区,IF=11.4)杂志发表了题为“Eicosapentaenoic acid enhances intestinal stem cell-mediated colonic epithelial regeneration by activating the LSD1-WNT signaling pathway”的研究论文,解析了n-3多不饱和脂肪酸调控肠道干细胞命运促进肠道再生的分子机制。

在现代集约化养殖中,多种不利因素如病原菌感染、应激等会导致动物肠道炎症,并伴随着肠道损伤、腹泻以及营养消化不良等问题,是造成动物生长缓慢的重要因素(SCIENCE CHINA Life Sciences,2023)。肠道干细胞是位于隐窝底部的多功能干细胞,具有分化为肠上皮细胞的潜力,也是驱动肠道损伤修复的主要动力来源(Trends in Cell Biology,2021;Nutrition Research Reviews,2022)。因而,调控肠道干细胞的增殖和分化对于缓解动物的肠道损伤具有重要意义。
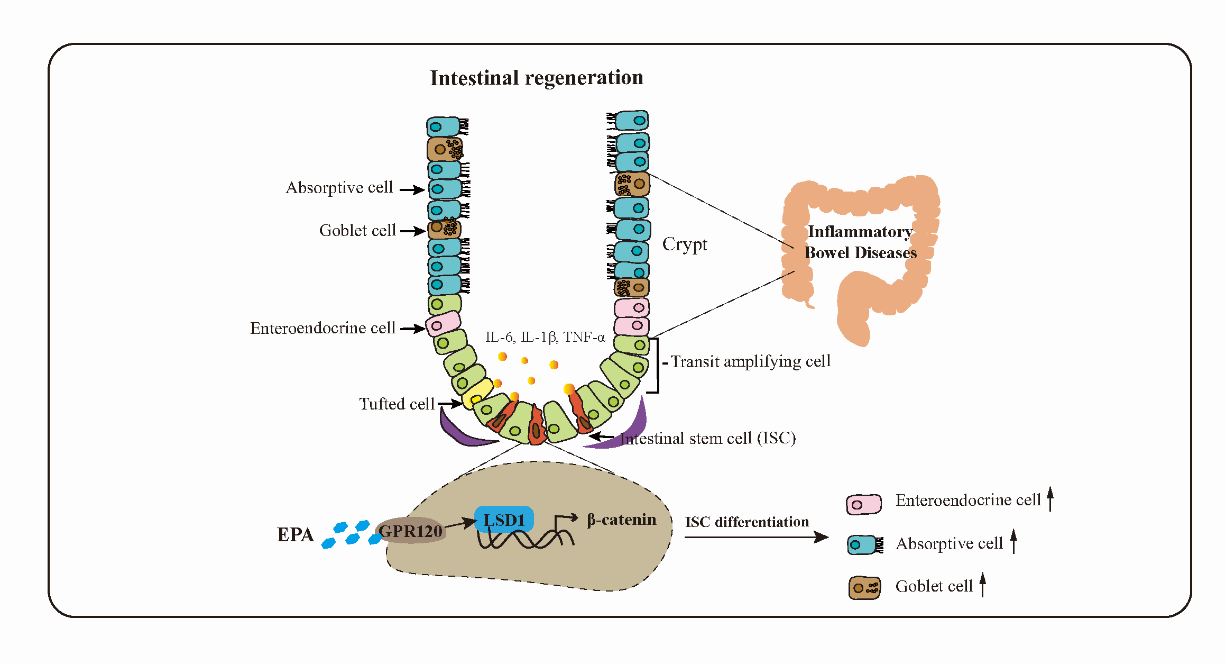
n-3多不饱和脂肪酸,如二十碳五烯酸(EPA)主要存在于深海鱼油,具有调节免疫反应、抗炎和降血压等多种生理功能。本课题组前期研究表明,n-3多不饱和脂肪酸能缓解脂多糖或呕吐毒素诱导的动物肠上皮细胞损伤(The FASEB Journal,2020),但其分子机制知之甚少。本研究以葡聚糖硫酸钠DSS诱导的结肠炎小鼠、肠道类器官或条件性敲除小鼠为模型,从肠道干细胞角度解析EPA在肠道再生中的作用和分子机制。研究发现,日粮中添加5%的EPA鱼油能显著缓解DSS诱导的急性结肠炎,并增加增殖细胞、吸收细胞、杯状细胞和肠内分泌细胞的数量进而促进肠上皮的再生;体外研究也证实,EPA预处理能促进肠道干细胞的增殖和分化,并保护肠道类器官免受TNF-α 诱导的损伤;在机制方面,EPA上调G蛋白偶联受体120(GPR120)并诱导组蛋白去甲基化酶LSD1表达,从而激活下游的WNT/β-catenin信号通路,进而促进肠道干细胞的增殖和分化;采用Loxp-Cre系统构建条件性敲除LSD1的小鼠模型后发现,肠道干细胞缺失LSD1能阻断EPA对DSS诱导的小鼠结肠炎的缓解作用。以上研究表明,EPA通过激活LSD1-WNT信号促进肠道干细胞增殖和分化,从而增强肠道上皮的再生能力。该研究从表观遗传修饰调控肠道干细胞命运的角度阐明了EPA促进肠道再生的新机制,研究有望为动物肠道损伤的精准营养调控策略提供了重要的理论依据。
我校动科学院王丹副教授和2022级研究生武念邦为该论文第一作者,刘玉兰教授为论文通讯作者,动物营养与饲料科学湖北省重点实验室为第一单位。本研究得到了国家自然科学基金区域创新发展联合基金重点项目(U22A20517)、国家自然科学面上基金(32472941)和青年项目(32102566)等项目的资助。
论文链接:https://linkinghub.elsevier.com/retrieve/pii/S2090123224006283